
特邀两位讨论嘉宾,他们是来自:临沂市人民医院刘丽丽教授;潍坊市中医院卢龙涛教授。
又将会围绕非小细胞肺癌
展开怎样的话题呢?
来让我们一探究竟吧!
专题一肺癌形态学诊断及WHO分类新进展
首先是来自山东大学齐鲁医院韩博教授,为我们带来肺癌形态学诊断及WHO分类的最新进展。
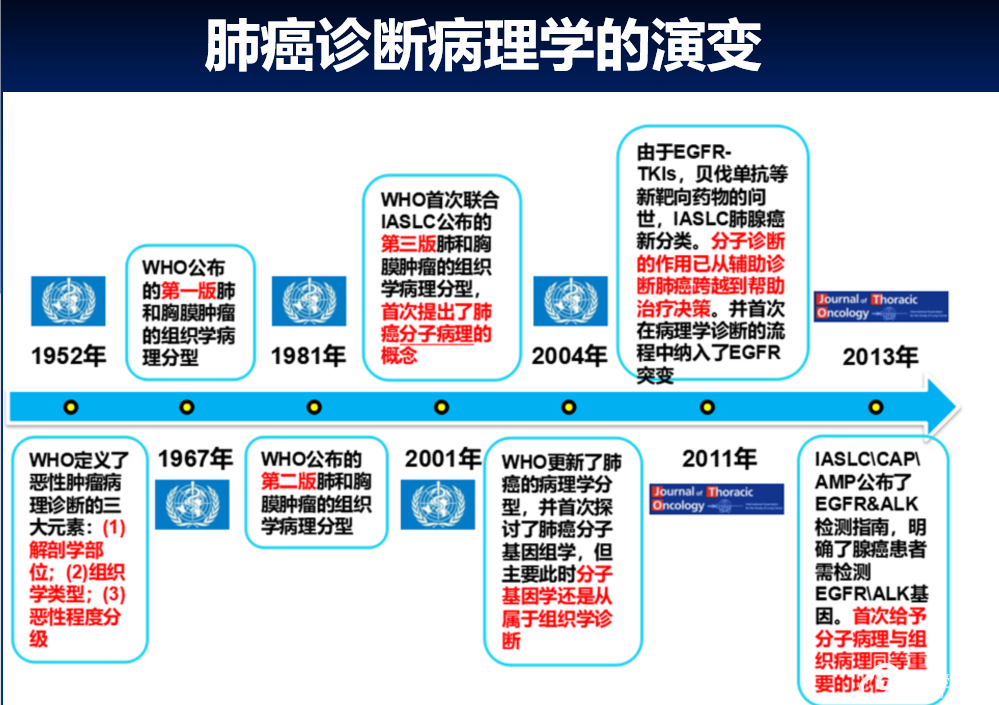

其中主要变化还为:
将肺腺癌分列为三类
浸润前病变
微浸润性腺癌
浸润性腺癌
提出原位腺癌(AIS)和微浸润性腺癌(MIA)的新概念。
弃用细支气管肺泡癌(BAC) 及混合型腺癌诊断术语,增加贴壁状为主型腺癌、微乳头状为主型腺癌、肠型腺癌。取消黏液性囊腺癌、印戒细胞癌、透明细胞癌。对小活检和细胞学标本 病理诊断提出新要求和标准:送检标本量和质量;诊断分型尽可能明确;推荐采用免疫组化和组织化学等。
强调了放射影像学对肺孤立性小结节的诊断价值和临床意义

非典型腺瘤性增生
浸润前病变,等同于鳞状上皮不典型增生5-23%的腺癌旁见到AAH分子生物学显示与肺腺癌相关基因改变相似(KRAS、EGFR突变, p53+, FHIT+, Wnt 通路表观遗传学改变等)
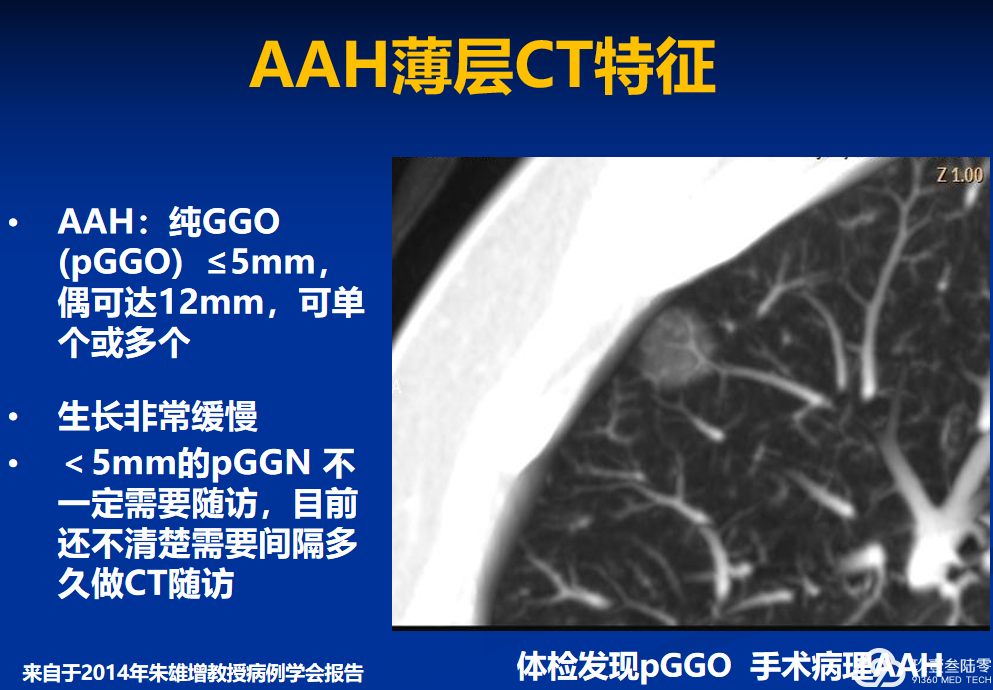
通常≤0.5 cm 肿瘤细胞沿肺泡壁呈贴壁状生长,细胞轻-中度非典型,“图钉”样,可有核内包涵体,细胞间有裂隙 ,AAH与AIS可以是一个连续过程,有时仅凭细胞学难以区分,AAH不再分高、低级别。
原位腺癌
浸润前病变一种肿瘤细胞严格地沿着以前存在的肺泡结构生长(贴壁状生长)局限性小(≤3 cm)腺癌,缺乏间质、血管和胸膜侵犯 ?相当于过去的纯BAC诊断标准(NOGUCHI分型的A和B型)无乳头或微乳头生长方式,肺泡腔内无瘤细胞AIS分为非粘液性和粘液性两型,后者极罕见
原位腺癌是不具有侵犯能的,病理诊断AIS的标准是十分重要 !!!
微浸润性腺癌
一种以贴壁状生长为主的孤立性小腺癌(≤3cm),任何一个病灶浸润的最大直径≤0.5 cm微浸润病灶判定标准:1. 组织形态为非贴壁状生长方式,可为腺泡状、乳头状、微乳头状和/或实性生长2. 肿瘤细胞浸润肌纤维母细胞的肺间质内如有淋巴管、血管或胸膜侵犯 ,或有肿瘤性坏死时,不再诊断MIA,应直接诊断为浸润性癌多灶浸润时,以最大一个病灶的直径为准
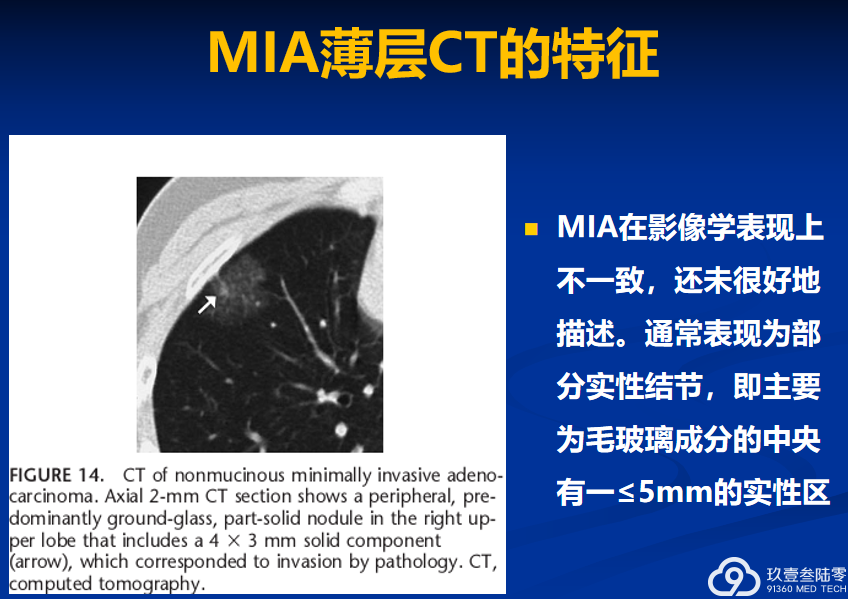
贴壁状为主(原来的非黏液性BAC生长方式,浸润灶>5mm)
腺泡性为主
乳头状为主
微乳头状为主
实性为主伴有黏液产物
浸润性腺癌变型

原位腺癌在WHO(2021)肺肿瘤组织学分类中,从肺腺癌的大类中分离出来,和非典型腺瘤样增生一样,被定义为腺体前驱病变。相当于癌前病变,不再属于肺腺癌中的一类。新增包括细支气管腺瘤、SMARCA-4-缺陷未分化肿瘤和原位间皮瘤等少见的肿瘤类型。侵袭性非粘液性肺腺癌的IASLC分级体系被提出,并将其纳入第5版的WHO胸部肿瘤分类中。

SMARCA4基因编码BRG1蛋白,是一个染色质重塑单位的催化亚基,涉及多种重要的生化功能。
2015年,Loarer等报道了一组高度侵袭性的胸部肉瘤,这组病例发生于成人男性,多具有横纹肌样形态,且均有体细胞性SMARCA4突变和免疫组化BRG1缺失。该组肿瘤常见TP53突变、肿瘤突变负荷高、无SMARCA4的胚系异常;常表达CD34、SALL4、SOX2,对常规治疗无效,常在数月内死亡。
近年来,SMARCA4缺失型非小细胞肺癌视为一种特殊的非小细胞肺癌亚型。免疫组化一般不表达TTF-1,常表达CK7、HepPar1。最近有研究提出SMARCA4缺失型胸部肉瘤是SMARCA4缺失型非小细胞肺癌中的未分化类型,但准确鉴别两者还是有显著意义,因为前者的预后更差。已有部分研究提示,这组肿瘤可能对免疫治疗有效。
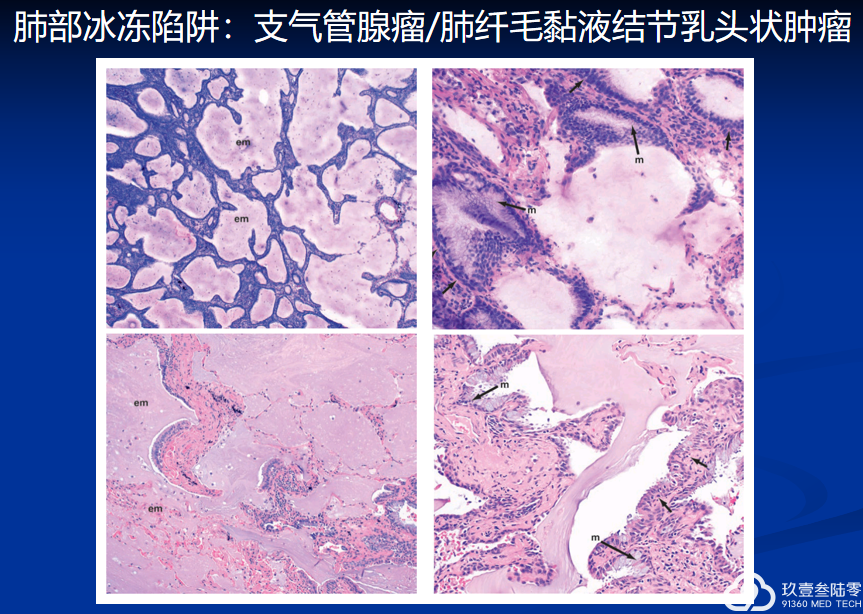
冰冻切片中,高倍镜下仔细评估有助于诊断性特征的发现,即形态温和的纤毛柱状上皮和黏液细胞混杂在一起,同时更重要的是包括基底细胞在内的双层细胞表现。了解这一病种及相关组织学表现,有助于避免诊断陷阱。
原位间皮瘤
是一种位于胸膜表面生长的非浸润性间皮肿瘤理论上,恶性间皮瘤可能由此阶段发展而来
临床表现
有限的病例报道显示,肿瘤均位于胸膜?好发于39~72岁间的中老年患者,男性多见 临床症状包括呼吸急促、胸痛和干咳,多伴有反复性胸水多数患者有石棉接触史。

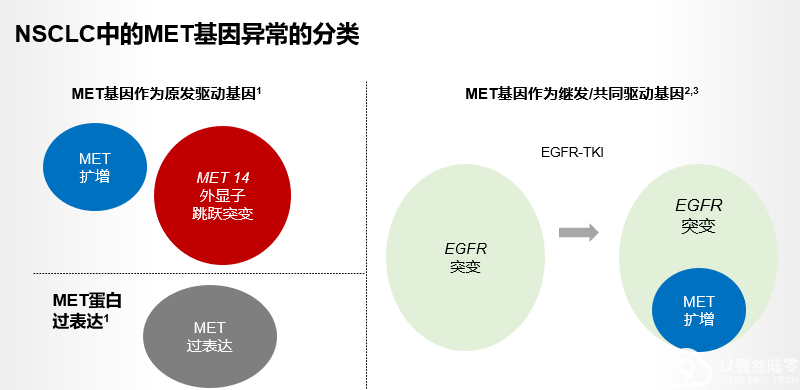
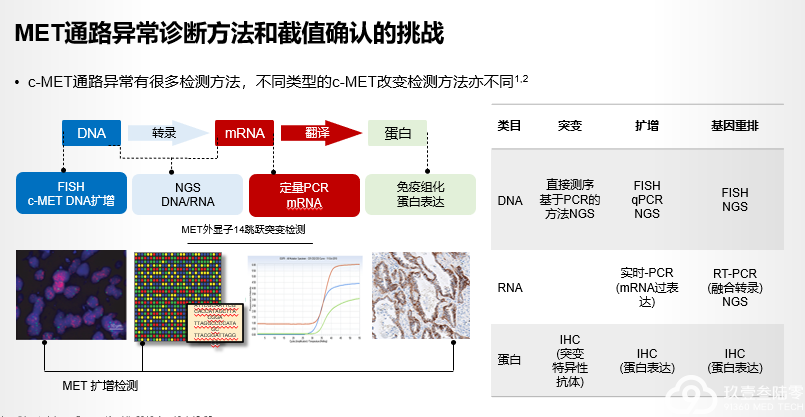
专题二 MET检测在NSCLC中的意义与方法
精准治疗离不开精准的检测,来自青岛大学附属医院 邢晓明教授为我们带来MET基因检测在非小细胞肺癌中的意义与方法。

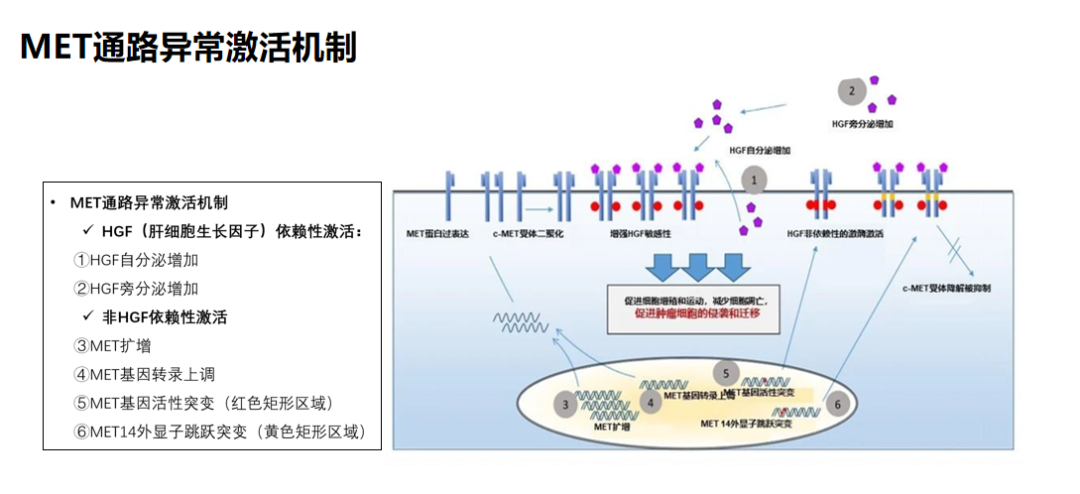
MET基因信号传导通路
首要环节:HGF与MET基因(SEMA区)特异性结合。
激酶激活:酪氨酸残基自身磷酸化,激活酪氨酸激酶。
下游多种信号通路被激活:
RAS-RAF-MAPK信号通路:参与细胞生长增殖
PI3K-AKT信号通路:参与细胞生存
PI3K-FAK信号通路:促进细胞迁移,具有侵袭特性
常见于老年(>70岁)、有吸烟史、晚期疾病的患者,预后不佳
与其他基因变异相互排斥,如EGFR、ALK、ROS1.
同时合并MET扩增:15%~20%3~4

细胞表面RTK聚集引起的EGFR致癌信号通路的解聚,促进MET介导的旁路信号通路的独特生化途径?(旁路激活)
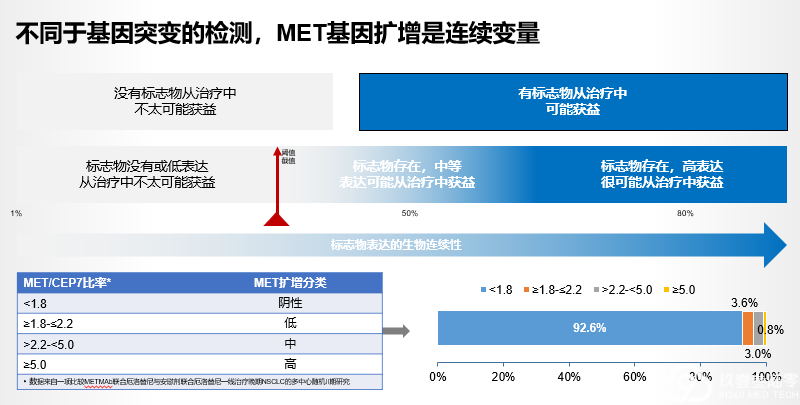
二、MET信号通路异常在NSCLC中的意义

在肿瘤细胞的胞质和细胞膜均可见cMET染色
磷酸化的cMET染色主要集中在面对肺泡间隙的膜上
病例分享1
H21-14152汪某某,女,58岁。(右肺下叶结节)微浸润性腺癌(范围0.9*0.8cm),未累及肺断端。免疫组化:TTF-1(+),NapsinA(+),ALK-D5F3(-),ALK-D5F3-N(-),Ki-67(+,5%),p40(-),CK7(+),p53(+,突变型),PD-L1-22C3(TPS:<1%),pan-Trk(-),CD8(+,约5%)。行NGS检测结果示:KIF5B-MET(K24:M15)融合?患者目前未接受任何辅助治疗。
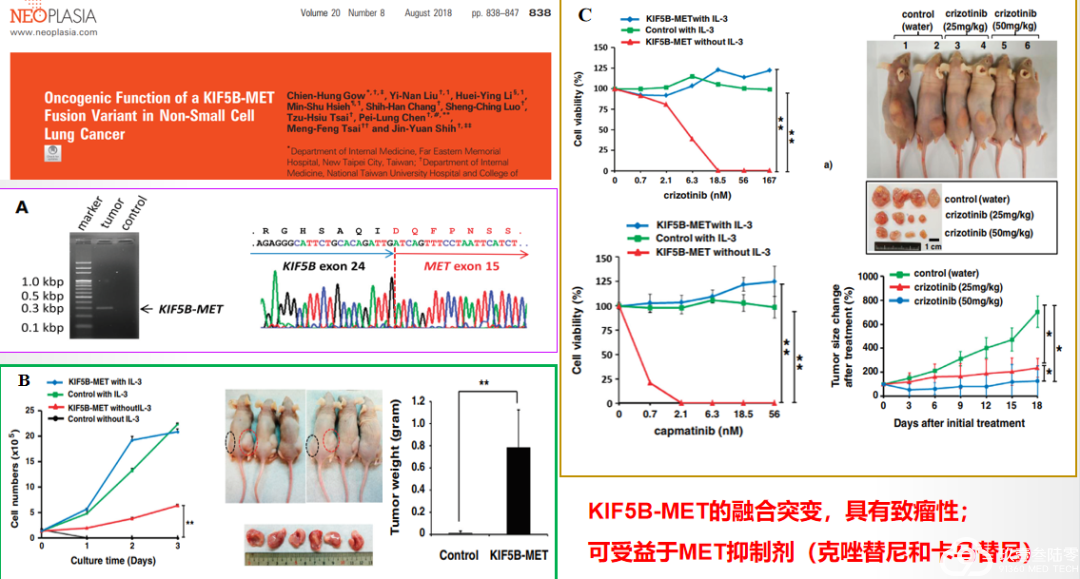
三、MET信号通路异常的靶向治疗进展

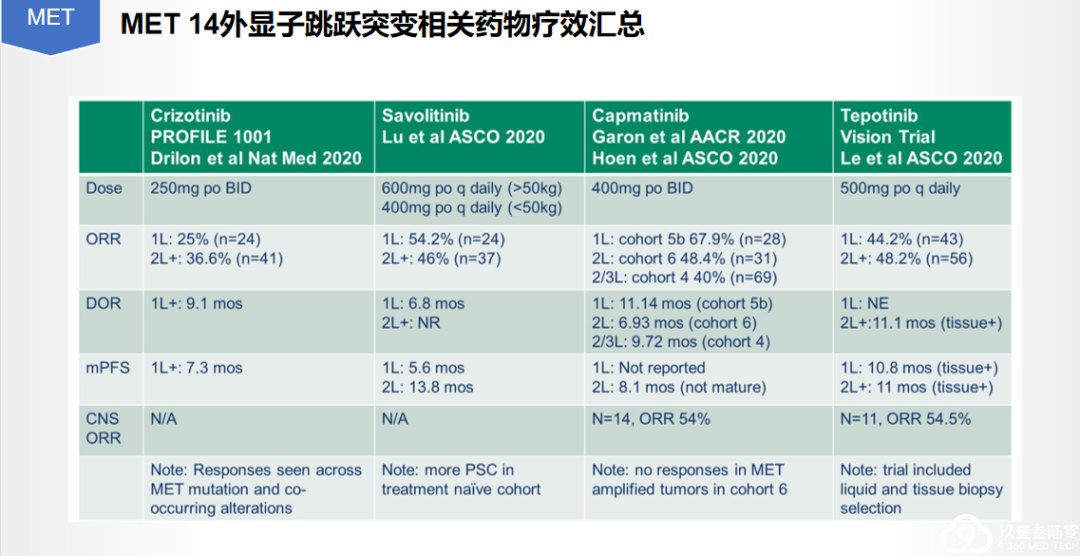 MET在NSCLC中的意义与检测方法:总结
MET在NSCLC中的意义与检测方法:总结MET作为NSCLC的驱动基因之一,已经得到越来越多的关注,成为近年来的研究热点。
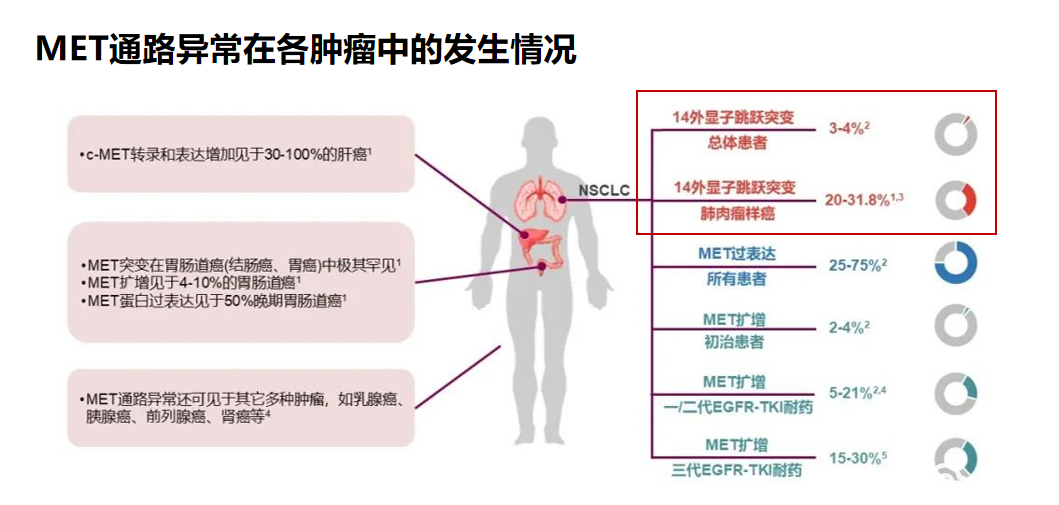
c-MET外显子14跳跃突变:重要的治疗靶点
c-MET外显子14跳跃突变在晚期NCLC的发生率为~3%,在肺肉瘤样肿瘤患者中可高达30%。
MET抑制剂的疗效与MET外显子14跳跃突变发生的区域无关。
采用RT-PCR、基于RNA或DNA的NGS的诊断方法具有高度的一致性。
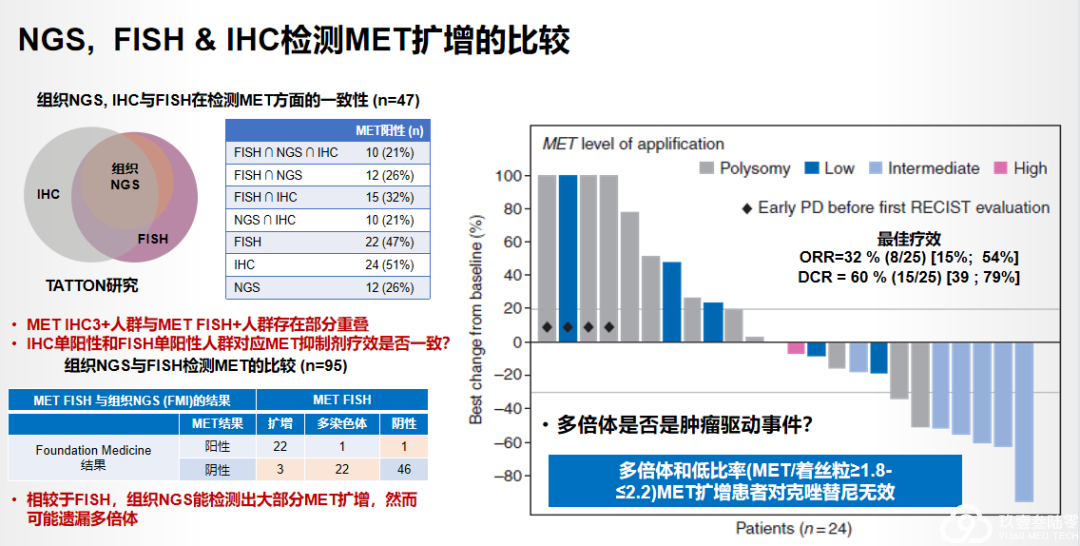
c-MET扩增:重要的耐药机制
c-MET扩增在接受过一、二代和三代EGFR-TKI治疗晚期EGFR突变患者的发生率分别为5%-22%和~19%。
FISH、NGS、IHC都可以用于MET扩增的检测,其中组织FISH是扩增检测的金标准。
MET扩增的血液检测,临床需求大但是技术仍不成熟。
MET基因是非小细胞肺癌中重要的基因之一,MET扩增是EGFR TKI耐药的重要机制之一。FISH、NGS、IHC都可以用于MET扩增的检测,临床研究显示扩增/表达水平越高,MET抑制剂疗效越好,液体检测也是选择之一。邢晓明教授为我们带来了精彩的专题分享。
专题三NGS助力MET突变NSCLC的精准治疗
来自潍坊市人民医院张云香教授,为我们带来NGS助力MET突变非小细胞肺癌的精准治疗。
NSCLC NCCN指南:首次增加MET Exon 14 skipping突变的治疗方案。
2020 NSCLC CSCO指南:
也将MET14外显子跳跃列入常规检测推荐
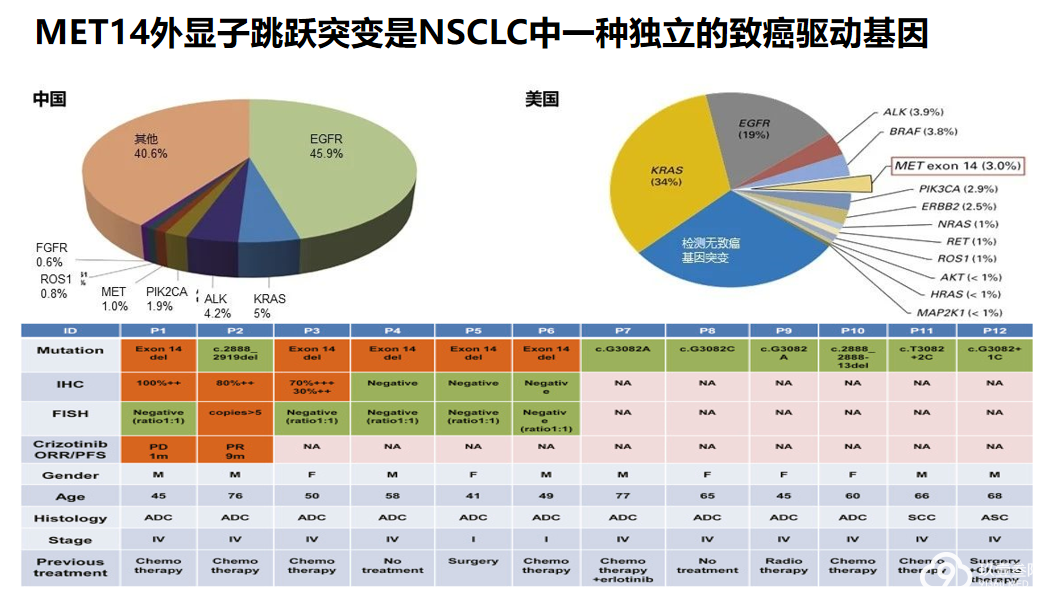
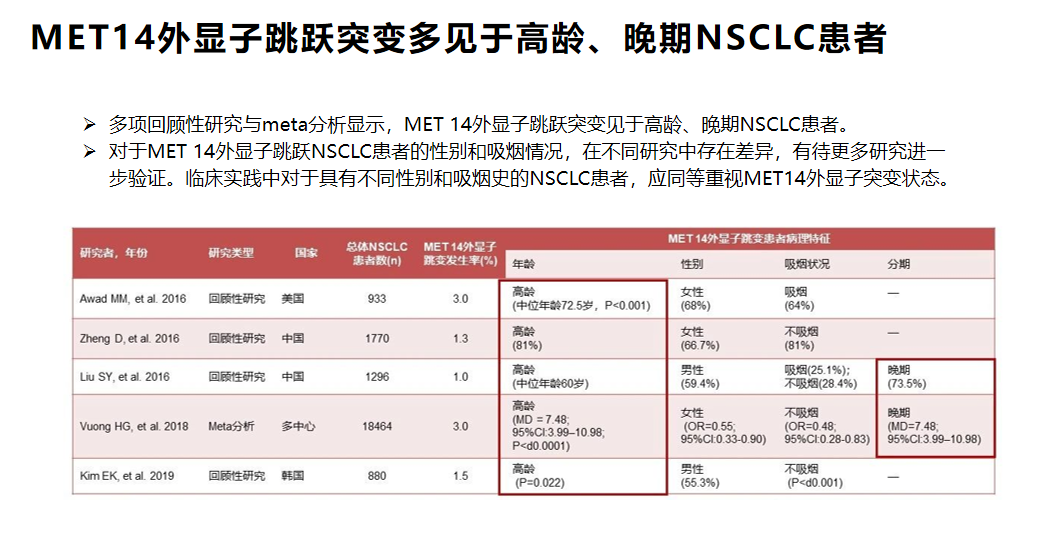
对于传统化疗,如没有EGFR突变进行化疗,MET14外显子跳跃突变中位OS只有半年。
对于免疫治疗,MET 14外显子跳跃突变患者中位PFS仅1-2个月。
三、雨后春笋
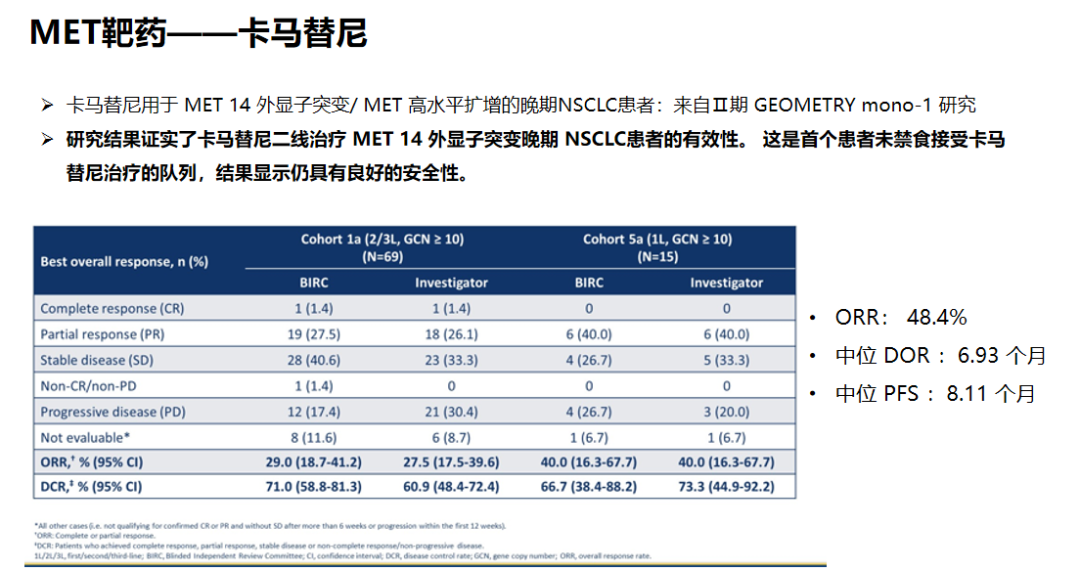
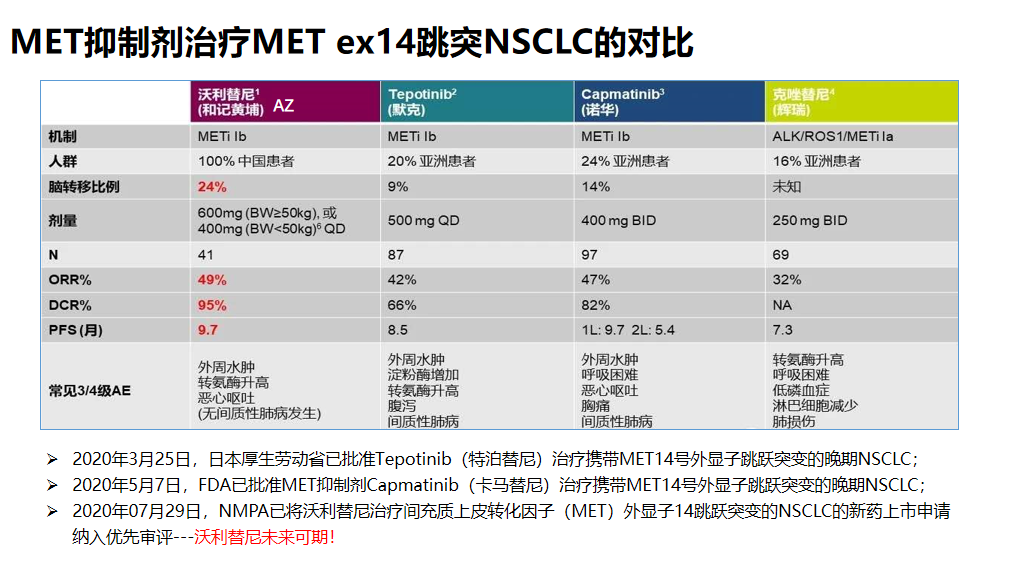
MET检测存在的难点
国内对于?MET 通路突变的临床检测率较低,CSCO 指南目前也暂无针对该突变的相关诊疗推荐
标本太少!c-Met 蛋白过表达通常采用免疫组化(IHC)进行检测,该技术需要较其他检测方法更多的标本量;
没有共识!对于 MET 扩增,常用的原位杂交(FISH)法阳性结果判定的cut-off值尚未达成共识,不同研究采用的截断值及高中低水平扩增标准不同;(5%?2%)
高度多样!由于 MET 14 号外显子跳跃突变具有高度分子多样性,包括:不等长度的碱基对缺失、点突变和插入缺失等,使得分子检测存在挑战。
MET重排的检测——FISH、IHC、NGS
FISH 或 IHC 是检测 MET 与 ALK、RET、ROS1、NTRK1 等基因重排的金标准检测方法;基于 RNA 的二代测序(NGS)检测重排是一种与上述两种方法等效的快速且可靠的替代方法。
重排低,可作为金标准。
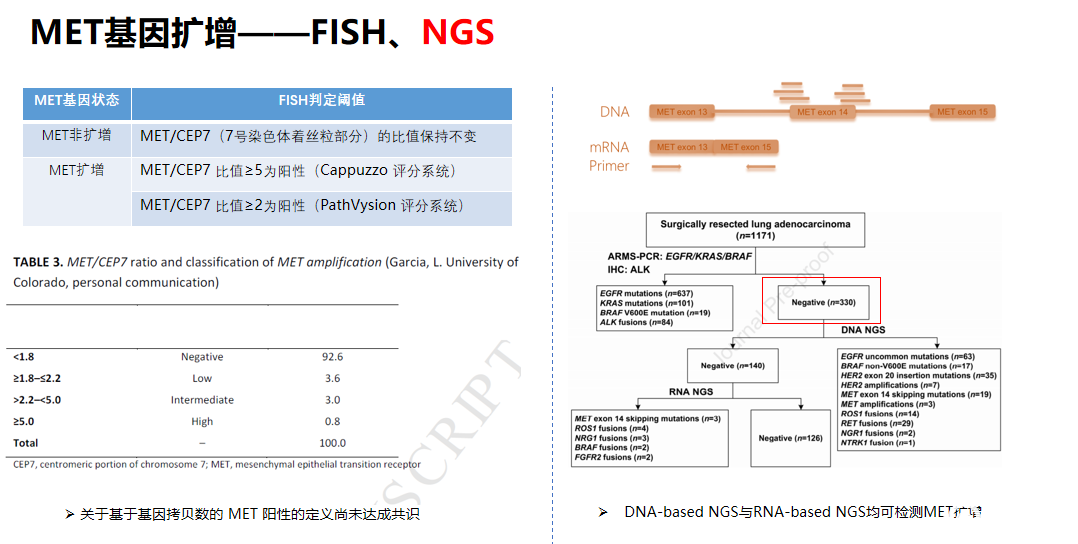

RNA-based NGS检测MET 14 skipping更全面!
NGS助力MET基因检测,张云香教授为我们从罕见突变MET及基因、MET成为NSCLC精准治疗的重要靶点、MET靶向药物及伴随诊断新进展以及MET的检测方法四个方面为我们带来了精彩的分享。
本次会议专家讨论要点
1、在什么情况下检测MET
2、对原位腺癌与微浸润腺癌临床处理有何改变?
专家讨论概要
1、肺癌NGS方法可一次做突变与扩增,现唯一遗憾为NGS可能会遗漏一部分阳性,对数据分析要求较高。
从临床中,一种为原发另一种为EGFR靶向治疗后可能出现耐药,此时MET基因更多的表现为扩增。
2、临床对此新分类认识在不断提升,对于毛玻璃结节临床的处理还是需要定期随访与及时的干预,基本原则把握结合对病变的认识,把握干预的时间,如出现微浸润可能会进展较快,如何干预与治疗也值得我们不断探讨。
本次区域肺癌诊疗病理基地巡讲会暂落下帷幕,精准治疗离不开精准的检测,分子病理已经成为临床中重要的环节,希望未来我们能走在分子病理的前列,为更多患者带来希望!

